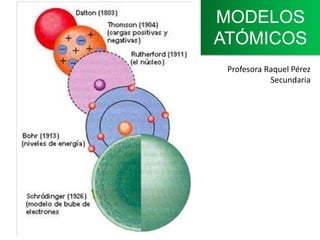
Modelos atómicos
- 2. DEMÓCRITO 460 a. C.-370 a. C. La materia está formada por átomos (del griego ἄτομον 'sin partes, indivisible') No es un modelo científico No fue tomado en consideración Teoría atomista La materia es discontinua
- 3. ARISTÓTELES 384 a. C.-322 a. C. La materia está formada por 4 elementos: tierra, aire, agua y fuego. No es un modelo científico Fue tomado en consideración durante 20 siglos La materia es continua Más tarde se añadió el éter o quintaesencia para explicar el vacío
- 5. MODELO ATÓMICO DE DALTON 1803 La materia está formada por átomos Los átomos son partículas indivisibles. La materia es discontinua Es el primer modelo científico
- 8. THOMSON Rayos catódicos Los rayos catódicos hacen girar una rueda de palas tienen masa Los rayos catódicos son desviados con campos electromagnéticos hacia la placa positiva tienen carga negativa Aparecen unos rayos luminosos que “salen” del cátodo (polo -): rayos catódicos Experimentos con tubos de descarga de gases. Gas encerrado en un tubo previamente vacío y sometido a una diferencia de potencial eléctrico. Los rayos catódicos son los electrones Si los átomos tienen electrones no son indivisibles
- 9. MODELO ATÓMICO DE THOMSON 1904 Masa + con e- incrustados: pastel de pasas
- 10. Tubos de descarga de gases Descubrimiento de los e-
- 12. RUTHERFORD Experimento Bombardea una lámina de oro con partículas a (carga +)
- 13. RUTHERFORD Experimento La mayor parte de las partículas atraviesan sin desviarse (lo esperado). Algunas se desvían Hay algo con carga + Unas pocas rebotan Hay algo con mucha masa Resultados esperados + Resultados obtenidos
- 14. MODELO ATÓMICO DE RUTHERFORD 1911 Neutrones n0 Núcleo Protones p+ Núcleo con partículas + y toda la masa Electrones girando en órbitas circulares a gran distancia Corteza: electrones e- +
- 15. PARTÍCULAS SUBATÓMICAS Carga y masa +
- 16. Tubos de descarga de gases Descubrimiento de los e- Experimento lámina de oro Algunas partículas a rebotan
- 17. BOHR 1885-1962
- 18. MODELO ATÓMICO DE BOHR 1913 Incorpora la mecánica cuántica: solo son posibles ciertos valores Distribución de los electrones: niveles y subniveles = orbitales
- 19. MODELO ATÓMICO DE BOHR 1913 Saltos de electrones entre niveles: emisión de energía (onda electromagnética) espectros atómicos
- 20. Tubos de descarga de gases Descubrimiento de los e- Experimento lámina de oro Algunas partículas a rebotan Mecánica cuántica Espectros atómicos
- 22. MODELO ATÓMICO DE SCHRÖDINGER 1926 Modelo mecanocuántico ondulatorio probabilístico De Broglie: los electrones se mueven como una onda Heisenberg: Imposibilidad de conocer la posición exacta de los e- probabilidad Nube de e-
- 23. Tubos de descarga de gases Descubrimiento de los e- Experimento lámina de oro Algunas partículas a rebotan Mecánica cuántica Espectros atómicos Movimiento ondulatorio de e- Imposible conocer posición e- Probabilidad
- 24. REPRESENTACIÓN DE LOS ÁTOMOS Número atómico y número másico Número atómico: número de protones Número másico: número de protones + neutrones
- 25. REPRESENTACIÓN DE LOS ÁTOMOS Ejercicio 13 14 10 ¿Cuántos protones, neutrones y electrones tienen?