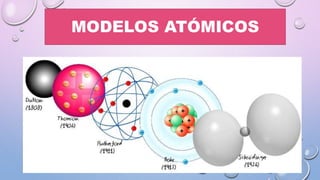
MODELOS ATÓMICOS
- 2. Cada uno de los objetos que puedes ver a tu alrededor ocupa un espacio y puede medirse. Estos objetos reciben el nombre de materia, por lo tanto, podemos decir que la materia es todo aquello que ocupa un lugar en el espacio y tiene masa. EL ÁTOMO
- 3. En el siglo V a. C., Demócrito postuló que la materia estaba formada por partículas muy pequeñas e indivisibles: los átomos. Estos no se pueden dividir, por tanto el átomo es la unidad constituyente más pequeña de la materia que posee las propiedades de un elemento químico.
- 4. TEORÍA DE DALTON En 1808, John Dalton enunció su célebre teoría atómica que justifica estos postulados. • La materia está formada por pequeñas partículas, separadas e indivisibles, llamadas átomos. • La materia que tiene todos sus átomos iguales es un elemento. • Los átomos de los diferentes elementos se distinguen por su masa y sus propiedades. • Los átomos de elementos distintos pueden unirse en cantidades fijas para originar compuestos. • Los átomos de un determinado compuesto o átomos compuestos son también iguales en masa y en propiedades.
- 5. Tres años más tarde, en 1811, el químico italiano Amadeo Avogadro denominó moléculas a los átomos compuestos de Dalton. MOLÉCULAS
- 6. TEORÍA DE THOMPSON La distribución de las cargas propuesta por Thomson explicaba la aparición de los rayos catódicos y los rayos canales donde se descubre que el átomo tiene cargas positivas y negativas El átomo es una esfera uniforme cargada positivamente donde se incrustaban cargas negativas El átomo tiene carga neutra Thompson considera al átomo como una gran esfera con carga eléctrica positiva en la cual se distribuyen los electrones como pequeños granitos. (en forma similar a las pepitas de una sandía o conocido también como el modelo del pudín de pasas)
- 7. TEORÍA DE RUTHERFORD El átomo está formado por dos partes el núcleo y la corteza En el núcleo se encuentran las cargas positivas o protones En la corteza se encuentran las cargas negativas o electrones El núcleo es muy pequeño en comparación con el tamaño del átomo y es donde se concentra la mayor parte del peso. El átomo es neutro porque tiene el mismo número de cargas positivas y negativas
- 8. MODELO DE NIELS BOHR Los electrones se desplazan alrededor del núcleo como un sistema planetario Los electrones giran alrededor del núcleo describiendo órbitas circulares Las órbitas tienen diferentes niveles de energía Los niveles que se encuentran cerca del núcleo tienen menos energía mientras que los niveles más alejados del núcleo tienen más energía El electrón absorbe o irradia energía cuando cambia de órbita Los electrones poseen energía y se mueven en forma de onda En cada órbita puede existir un determinado número de electrones
- 9. MODELO DE SOMMERFELD El electrón puede moverse en forma elíptica a partir del segundo nivel de energía
- 10. ACTIVIDADES A REALIZAR Realizar una lectura comprensiva del texto del MINEDUC de primero de bachillerato pg. 18-30 Guiarse por la ficha de actividades de la semana 4 Analizar las presentaciones en PowerPoint con la información sobre MODELOS ATÓMICOS Observar el video compartido sobre la temática tratada https://www.youtube.com/watch?v=KAi3pjk2u7w Todo el material de apoyo puede encontrar en el aula virtual uehuasimpamba.com
- 11. TAREA Desarrollar la siguiente tarea una hojita de papel. Dibuja cada modelo atómico y escribe la característica más importante de cada modelo. UNIDAD EDUCATIVA HUASIMPAMBA Nombre……. Docente: Mg. Elena Paredes Curso y Paralelo………. Semana……………….. Fecha……………… Tema: MODELOS ATÓMICOS